-
125

- 권호정 교수팀, 신규 오토파지 유도제 발견과 타우병증 단백질 분해 활성 규명
- 신규 오토파지 유도제 발견과 타우병증 단백질 분해 활성 규명 FDA 승인 약물 2,896 종을 활용해 오토파지를 유도하는 약물 고효율 탐색 알츠하이머 치매의 원인 물질 중 하나인 타우 단백질 분해 효과 및 표적 기전 규명 [사진: (왼쪽부터)권호정 교수, 황희윤 연구원, 김다솔 연구원] 권호정 교수(생명공학과) 연구팀이 임상약 라이브러리 2,896 종을 활용해 오토파지를 효과적으로 유도하는 약물로서 항우울제인 서트라린(sertraline)을 오토파지 표현형에 근거한 고효율 탐색법으로 발견했다. 오토파지 조절 이상에 의한 관련 질병으로는 신경퇴행성 질환, 암, 노화, 대사성 질환 등이 알려져 있으며, 따라서 본 질환을 효과적으로 조절하기 위해 오토파지를 조절하는 약물을 발견하고 그 기전을 규명하는 것이 전 세계적으로 주목 받고 있다. 본 화합물은 임상적으로 안정성 및 독성 평가가 완료됐기 때문에 새로운 활성의 약물 개발에 있어 장점을 가지고 있다. 연구팀은 서트라린의 오토파지 유도 활성을 형광면역염색 및 작용인자 발현 분석을 통해 확인했다. 나아가 생물정보학적/생물리학적/생물학적 결합 검증 방법, 가상도킹모델 시스템을 활용해 서트라린이 미토콘드리아 외막의 이온 통로로 알려진 VDAC1 단백질과 직접적으로 결합함을 확인했다. 또한 서트라린이 VDAC1과 직접적인 결합을 통해 AMPK-MTOR 신호전달체계를 조절함으로써 오토파지 활성을 유도함을 규명했다. 나아가 서트라린은 타우병증 세포 모델에서도 효과적으로 오토파지를 유도했고, 그 결과 알츠하이머의 원인 물질 중 하나인 타우(tau) 단백질을 분해함으로써 타우병증을 효과적으로 억제할 수 있음을 제시해 본 약물이 새로운 오토파지 유도 약물로서 타우병증의 효과적인 치료제로서 개발될 수 있음이 시사됐다. 이번 연구성과는 과학기술정보통신부-한국연구재단이 추진하는 기초연구사업(글로벌연구실사업)의 지원으로 수행됐으며, 국제학술지 ‘오토파지(Autophagy, SCI)’에 11월 9일 게재됐다. 본 학술지는 최근 5년 간의 평균 IF 11.996으로 분야 Q1의 최우수학술지이다. [그림: A) 서트라린의 오토파지 유도활성. B) 가상도킹모델을 활용한 서트라린과 신규 표적단백질 VDAC1 간의 결합 검증. C) 서트라린의 타우 단백질 제거 활성. D) 서트라린의 오토파지 유도 및 타우병증 억제 기전 모식도.] 용어설명 ● 오토파지(Autophagy): 세포 내 구성요소의 파괴와 재활용에 질서를 제공하는 세포 구성 성분을 자연적으로 분해하는 파괴 기전. 세포 내 영양분이 부족하거나 외부에서 미생물이 침입했을 때와 같은 스트레스 상황에서 세포 스스로 생존을 위해 내부 단백질을 재활용해 항상성을 유지하는 자가 방어 기전. ● 서트라린(Sertraline): 선택적 세로토닌 재흡수 억제를 위한 항우울제. 1991년 미국 화이자사가 시장에 도입해 미국 연방 식품 의약품국 (FDA)이 승인. ● VDAC1 (Voltage-dependent anion-selective channel 1): 미토콘드리아 외막에 형성된 이온 채널. ATP가 미토콘드리아에서 세포질로 확산되도록 역할을 함. ● 타우(Tau): 뇌세포의 염색체 이동 및 세포의 구조를 유지하는 역할을 하는 미세소관(Microtubule)을 이루고 있는 단백질. ● 타우병증(Tauopathy): 퇴행성 신경질환의 원인 물질로 알려진 타우 단백질의 축적으로부터 발생하는 질환. 타우 단백질에 인(phosphate)이 과도하게 부착되는 변형이 발생하면 응집하여 신경섬유농축체(neurofibrillary tangle)를 형성하고, 이는 뇌신경 세포를 손상시킴으로써 병변을 일으킴. 논문정보 논문명: Antidepressant drug sertraline modulates AMPK-MTOR signaling-mediated autophagy via targeting mitochondrial VDAC1 protein 저널명: Autophagy 키워드: AMPK, DARTS, 타우(tau), 타우병증(tauopathy), VDAC1 DOI: 10.1080/15548627.2020.1841953 저 자: 권호정 교수(교신저자, 연세대), 황희윤(제1저자, 연세대), 심중섭 교수(공저자, Macau University, 중국), 김다솔(공저자, 연세대)
- 생명공학과 2020.11.19
-
124

- 조승우 교수 연구팀, 곤충의 외골격 형성 과정을 모사한 초강력 접착제 개발
- 연세대학교 생명공학과 조승우 교수 연구팀은 한국과학기술원 화학과 이해신 교수 연구팀과 공동연구를 통해 곤충의외골격 형성 과정에 관여하는 페놀기와 아민 작용기 사이의 생화학 반응을 모사한 초강력 접착제를 개발하였다. 본 연구에서는 뛰어난 반응성으로 자연산화가 가능한 갈롤기를 페놀기 유도체로, 다양한아민을 포함한 폴리에틸렌이민을 고분자 구조체로, 추가적인 산소를 공급하면서 구조적 강도를 부여할 수있는 실리카 나노파티클을 반응 촉진제로 활용하여 빠르고, 안전하며 강력한 친환경 접착제 (phenol/polyamine superglue; PPS)를 개발하였다. PPS는 수용성으로 제작되므로 휘발성 유기화합물이 방출되지 않기 때문에기존 접착제의 가장 큰 문제인 환경오염과 호흡기 독성 이슈를 해결하였으며, 표면의 성질에 국한되지 않고접착력을 가지는 갈롤기 덕분에 폴리염화비닐, 폴리카보네이트, 우레탄, 티탄, 섬유 등 대부분의 산업용 자재에 강력한 접착이 가능하다. 또한, 수용성 접착제 임에도 불구하고 접착원리가 비가역적 반응이기때문에 접착이 완료되면 탁월한 안전성과 빠르고 강력한 접착력을 기반으로 의료용 액상 반창고로서 활용 가능하다. 따라서, 개발된 생체모방 초강력 접착제는 표면의 특성에 제한되지 않는뛰어난 접착성과 안전성으로 일반생활 용품부터 의료용 제제에 걸쳐 다양한 산업 전반에 걸쳐 활용이 가능할 것으로 기대된다. 이번 연구는 전은제 대학원생이 주저자로 참여하여, 융합 소재 분야세계 최고 권위의 학술지 중 하나인 Advanced Materials (2019년 Impact factor: 27.398) 저널에 게재되었고, 연구 내용의중요성과 우수성을 인정받아 Advanced Materials 10월호 표지 논문으로도 선정되었다 (논문 제목: A Phenol-Amine Superglue Inspired byInsect Sclerotization Process).
- 생명공학과 2020.10.29
-
123
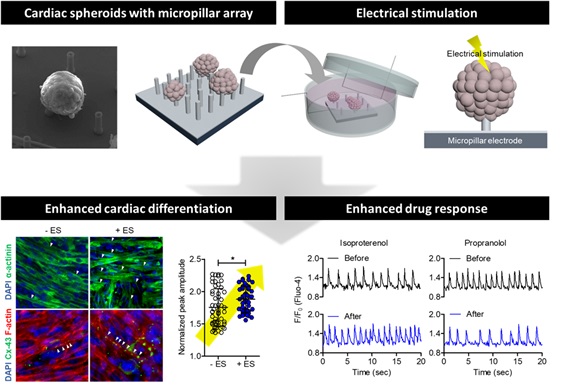
- 조승우 교수 연구팀, 심장 스페로이드 (spheroid)의 기능성 및 약물 반응성 증진 기술 개발
- 연세대학교 생명공학과 조승우 교수 연구팀은 전도성 미세기둥 디바이스를 제작하고 이를 이용한 전기자극을 통해 심장 스페로이드 (spheroid)의 기능성 및 약물 반응성을 증진시킬 수 있는 기술을 개발하였다. 본 연구 논문에서는 저분자 화합물의 처리를 통해 심장 리프로그래밍을 시도하여, 약물 스크리닝에 더욱 적합한 삼차원 심장 스페로이드를 효율적으로 제작하는 기술을 개발하였고, 기존의 방법보다 리프로그래밍의 효율이 증진된 것을 확인하였다. 이러한 삼차원 스페로이드 모델은 증진된 심장 기능성을 보여주고 약물 평가가 용이한 장점이 있지만, 삼차원 구조로 인해 효율적으로 전기자극을 인가하는 데에는 한계가 있었다. 따라서, 본 연구에서는 이러한 기존 전기자극 기술의 한계를 극복하기 위해 마이크로 수준의 정밀한 미세기둥 어레이를 제작하였고 심장 스페로이드를 미세기둥에 꽂아 심장 박동을 모사한 전기자극을 인가하여 심장 스페로이드의 분화능과 기능성 증진을 유도하였다. 또한, 전기자극을 통해 향상된 기능성을 가지는 심장 스페로이드가 심장의 박동을 조절할 수 있는 세 가지 약물에 대해 효과적으로 반응함을 확인함으로써, 심장 체외모델로서 약물 반응성 및 민감도도 증진된 것을 확인하였다. 일련의 결과를 통해 제작된 심장 스페로이드가 약물 평가에 활용될 수 있으며, 제작된 디바이스가 다양한 삼차원 세포 구조체에 대한 전기자극 플랫폼으로서 적용될 수 있음을 보고하였다. 본 연구는 연세대학교 신소재공학과 최헌진 교수 연구팀과 공동으로 수행되었으며 나노융합 분야 최고 수준의 학술지인 Nano Letters (2019년 Impact factor: 11.238) 저널에 9월 2일 온라인 게재되었고, 생명공학과 민성진 대학원생이 주저자로 참여하였다. (논문 제목: Biphasic Electrical Pulse by a Micropillar Electrode Array Enhances Maturation and Drug Response of Reprogrammed Cardiac Spheroids)
- 생명공학과 2020.10.05
